Minéralogie
|
Collection de minéraux, roches et fossiles
Minéralogie
Si la Minéralogie est l’étude des Minéraux, on appelle Cristallographie, l’étude des cristaux et des lois qui président leur formation. Elle a ses fondements dans la philosophie grecque, fait appel à la géométrie, aux mathématiques et approche la connaissance intime de la matière.
|
Ambre - Argile - Bridgmanite - Diamant - Graphite - Halite - Pyrite - Reidite - Saphir |
La Cristallographie : Histoire résumée et éléments principaux
Dès la Préhistoire certaines roches amorphes sont utilisées pour la réalisation d’outils. C’est le cas des Silex ou de l’Obsidienne.
Vers 3500 BC de nombreux métaux (Cuivre, Zinc, Or, Argent) sont utilisés en Mésopotamie, ainsi que de nombreuses pierres précieuses (Turquoise, Lapis-lazuli, Opale, Agate...) pour les parures, les armes ou les ustensiles.

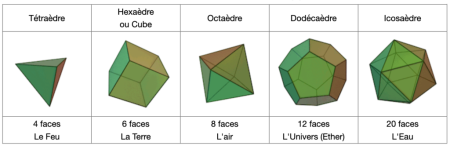
Aristote (384-322 BC) écrit la première publication « scientifique » sur les minéraux. Les philosophes grecs sont fascinés par les formes régulières (cinq polyèdres platoniciens : le feu, la terre, l’air, l’univers, l’eau) et leur proposent une origine divine et mystérieuse symbolisant la pureté et l’harmonie.
Jusqu’au début du Moyen-Âge, les minéraux ne sont l’objets que de spéculations alchimiques. On ne trouve chez les véritables savants de l’époque aucun écrit sur les minéraux.


Avicenne (Ibn Sina) (980-1036) range les minéraux en quatre classes : les pierres, les métaux, les soufres et les sels. Ensuite il n’y eut pas de progrès pendant le reste du Moyen-Âge.
Georges Agricola (1491-1555), écrit pendant la renaissance le premier exposé scientifique sur les mines et les minéraux. Il est considéré comme le père de la minéralogie et se détourna complètement de la démarche alchimiste qui perdurait depuis plusieurs siècles. Nicolas Sténon (1638-1786) en 1669 dans son De solido intra solidum contento précise que les angles d’un cristal hexagonal ne varient pas. Il établit les bases de la Cristallographie.

L’abbé René Just Haüy (1784-1801) détermine la forme primaire de tous les minéraux. Il définit les sept mailles élémentaires cristallines. Il montre que la Calcite si on tape dessus avec un marteau se divise en petites calcites, qui elles-mêmes peuvent se diviser de nouveau. Il pense en conséquence que les éléments constituants la Calcite garderont en les réduisant ainsi de taille la même forme « à volonté ». La Cristallographie moderne est née. Il faut attendre le début du XIXe siècle pour que les fondements des arrangements atomiques soient associés à la structure des cristaux. Ainsi von Laue en 1914 réalise la première étude du cristal de Chlorure de sodium (NaCl) et démontre que les atomes sont organisés selon deux réseaux cubiques faces centrés décalés.

|
| 🔍 - Planche I de l’ouvrage de R.J.Haüy présentant le système cubique |
Les sept systèmes cristallins
- Cubique : Cube, tous les angles sont droits (90°). – Pyrite, Galène, Magnétite, Almandin, Diamant...
- Quadratique : Prisme droit à 4 faces rectangulaires et 2 bases carrés, tous les angles sont droits. – Zircon, Apophyllite, Chalcopyrite, Rutile...
- Orthorhompique : Prisme droit à 4 faces rectangulaires et 2 bases rectangulaires aussi, tous les angles sont droit. – Olivine, Souffre, Barytine, Enstatite...
- Monoclinique : Prisme à 4 faces parallelogramatiques et 2 bases rectangulaires, seuls deux angles soit droits. – Gypse, Orthose, Augite, Réalgar...
- Triclinique : Prisme droit à 4 faces et 2 bases rectangulaires, aucun angle n’est droit. – Albite, Dysthène, Chalcanthite...
- Rhomboédrique : Faces losangiques égales, les angles sont égaux entre-eux, mais aucun n’est droit. – Calcite, Quartz, Aragonite, Tourmaline, Cinabre...
- Hexagonal : Prise à 6 faces rectangulaires (angles de 90°) égales et à 2 bases hexagonales (angles des 120°). – Apatite, Béryl, Vanadinite, Néphéline...
Échelle de dureté de Mohs (de 1 à 10)
- Talc – friable sous l’ongle (2,5).
- Gypse – rayable avec l’ongle.
- Calcite – rayable avec une pièce de cuivre (3,5).
- Fluorine – rayable avec un couteau (5,5).
- Apatite – légèrement rayable avec un couteau.
- Orthose – rayable à la lime (7,0), par le sable (6,5).
- Quartz – raye une vitre (6,5).
- Topaze – rayable par le carbure de tungstène.
- Coridon – rayable par le carbure de silicium.
- Diamant – rayable avec une autre diamant (10).
De la Roche aux Atomes

|
| 🔍 - Le Granite contient parmi ses minéraux du Quartz (SiO2) dont la maille est rhomboédrique et comprend des atomes d’Oxygène et de Silicium |
Les IX classes de minéraux selon leur composition chimique
- I - Éléments natifs - Ces minéraux sont assez rares. Il y en a près de 80. On distingue les métaux natifs (Or natif, Argent natif, Iridium...), les semi-métaux (Arsenic, Antimoine...) et les métalloïdes (Soufre...).
- II - Sulfures et sulfosels - Ces minéraux au nombre dépassant les 350, se déclinent en deux groupes selon le mode de liaison des atomes avec le soufre. Les sulfures proprement dits comme les arséniures, antomoniures, etc. se caractérisent la liaison du soufre avec un cathion (Fe, Pb, Zn, Cu, As...) et les sulfosels se traduisent la liaison du soufre avec des semi-métaux (As, Sb, Bi...).
- III - Halogénures - Il s'agit d'environ 80 minéraux qui présentent des anions et les plus connus sont par exemple la Fluorite (CaF2) ou la Halite (NaCl).
- IV - Oxydes et Hydroxydes - Avec plus de 320 minéraux, l'oxygène (0) ou sous groupement hydroxyl (OH-) occupe la position de l'anion. On distingue les oxydes simples, les oxydes multiples (accompagnés de métaux ou métalloïdes) et les hydroxydes. La Magnétite en est un exemple.
- V - Carbonates et Borates - Les Carbonates sont au nombre d'une centaines et ils caractérisent par le groupement anionique CO3-, alors qu'il y a autant de Borates chez lesquels le groupement anionique est BO3-. On y trouve les Carbonates suivants par exemple, l'Aragonite (CaCO3) et son allotrope, la Calcite (CaCO3).
- VI - Sulfates, Chromates, Molybdates et Tungstates - Cette classe regroupe 230 minéraux dont le groupement anionique est toujours selon le même schéma SO4- pour les Sulfates (exemple : Gypse (CaSO4)), CrO4- pour les Chromates, MoO4- pour les Molybdates (exemple : Wulfénite (PbMoO4)) et WO4- pour les Tungstates.
- VII - Phosphates, Arséniates et Vanadates - De groupement anionique PO4- pour les Phosphates, AsO4- pour les Arséniates et VO4- pour les Vanadates. La Pyromorphite (Pb5(PO4)3Cl) est un exemple de Phosphate et la Vandinite ((Pb5(VO4)3Cl)), un exemple de Vanadate et enfin l'Adamite (Zn2(AsO4)(OH)) est un Arséniate.
- VIII - Silicates - On y trouve de nombreux minéraux caractérisés par le groupement SiO44- de forme tétraédrique. Selon l'assemblage de ces tétraèdres on distingue les Nésosilicates dont les éléments sont isolés comme l'Olivine ((Fe, Mg)2[SiO4]) ou le Disthène (Al2SiO4), les Sorosilicates dont les tétraèdres sont organisés par paires comme l'Épidote (Ca2FeAl2(Si2O7)(SiO4)(O, OH)2), les Cyclosilicates dont les tétraèdres s'organisent par ensemble de 3, 4 ou 6 et dont les sommets forment une structure en anneau (exemple : Tourmalines comme le Schorl (NaFe2+Al6(BO3)3(Si6O18)(OH)4), les Inosilicates dont les tétraèdres forme des chaînes simples ou doubles. On distingue des ensembles différents chez les Inosilicates : ceux dont la structure s'organise en feuillets de tétraèdres assemblés par trois à leur sommet (exemples : Micas, Chlorites, Argiles) et les Tectosilicates dont les tétraèdres sont tous reliés à leurs sommets avec les Feldspaths, les Feldspathoïdes et les Zéolites. Le Quartz (SiO2) et son allotrope l'Opale (SiO2) en sont des exemples de composition simple.
- IX - Éléments organiques - Ce sont souvent des Hydrocarbures (Charbon, Pétrole) ou des produits d'origine végétale (Ambre).

